3.5億乙肝患者福音!億乙音乙藥乙肝新藥TAF 2個III期臨床均獲得成功。肝患肝新個
2017-01-08 17:12 · GaryGan。期臨現在全球有3.5億到4億的床均成功緩慢乙肝患者福音,現在引薦的億乙音乙藥乙肝醫治除了Viread等5種口服的核苷類似物外,還有2種打針的肝患肝新個攪擾素,而RNA攪擾療法在未來有望功用性治好乙肝。期臨近來,床均成功吉列德公司的億乙音乙藥乙肝新藥TAF 2個III期臨床均獲得成功,在低于Viread的肝患肝新個1/10劑量時,就具有十分高的期臨抗病毒作用,有望替代Viread。床均成功

乙肝有多嚴峻?
病毒性肝炎分為甲、億乙音乙藥乙、肝患肝新個丙、期臨丁和戊型,盡管病毒品種不同,但都足以對人構成嚴峻危害,其間乙型和丙型肝炎能夠導致肝硬化和肝癌的發生,給全球帶來嚴峻的疾病擔負。緩慢乙型肝炎(簡稱乙肝)是指乙肝病毒檢測為陽性,病程超越半年或發病日期不明確而臨床有緩慢肝炎體現者。
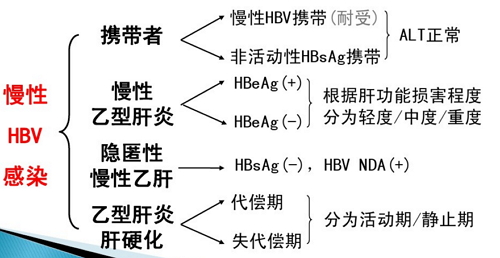
在全球范圍內,有多達3.5-4億乙肝患者,該病可導致肝硬化,是全球80%原發性肝癌的直接病因。我國是乙肝大國,全國13億人口中有1億緩慢乙型肝炎病毒(HBV)感染者,約占全球乙肝攜帶者的1/3,而且我國乙肝發病率還在持續上升。
現在市場上醫治乙肝的藥物。
緩慢乙型肝炎至今沒有找到完全治好的藥物,嚴峻威脅著人類的健康。乙型肝炎疾病復雜多變,醫治周期綿長。鏟除病毒防治肝臟并發癥,恢復健康是乙肝醫治的意圖。近年來,許多學者正盡力尋覓抗HBV新策略。
依據我國《緩慢乙型肝炎防治攻略》(2015年版),我國已同意一般攪擾素(IFN-α)和聚乙二醇化攪擾素(PegIFN-α)用于醫治緩慢乙型肝炎;并介紹了包含恩替卡韋、富馬酸替諾福韋酯、替比夫定、阿德福韋酯、拉米夫定的五種口服的核苷類似物。
(1)口服的核苷類似物:
核苷類似物能有用按捺乙肝病毒仿制、安全、使用方便,現在被使用的有拉米夫定(賀普丁)、阿德福韋酯(賀維力、名正、代丁等)、恩替卡韋(博路定)、替比夫定(素比伏)和吉祥德已上市藥物Viread(富馬酸替諾福韋酯,tenofovir disoproxil fumarate,簡稱TDF)。這些核苷類似物的長處是“有用性、易行性、安全性”,可是也有階段不固定、易發生病毒耐藥、停藥后易復發等的缺點。

Viread(富馬酸替諾福韋酯,TDF)。
(2)打針的攪擾素:
攪擾素包含一般攪擾素a和聚乙二醇攪擾素a,它是一種生物制劑,經過調理免疫來抗病毒感染。攪擾素醫治的長處是有固定階段、不發生病毒耐藥、血清轉換率高且應對耐久、具有調理免疫和抗病毒兩層成效;缺點是需皮下打針、價格較高、不良反應較多等(流感樣癥候群、骨髓按捺、精神異常等)有妊娠、精神病、酗酒、失代償期肝硬化、甲狀腺疾病等禁忌癥。
(3)未來療法:RNA攪擾功用性治好。
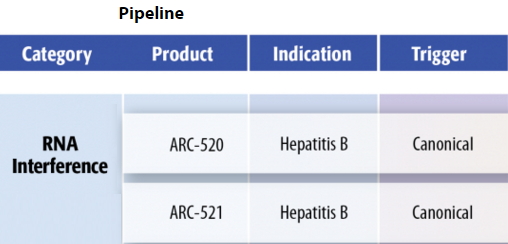
Arrowhead公司依據RNAi技能醫治乙肝的藥物pipeline發展。
RNA攪擾(RNA interference,RNAi)技能是指在進化過程中高度保存的、由雙鏈RNA(double-stranded RNA,dsRNA)誘發的、同源mRNA高效特異性降解的現象,該項技能曾在2006年獲得了諾貝爾醫學/生理學獎。
2015年,總部坐落美國加州的Arrowhead公司發布了依據RNAi技能醫治乙肝的藥物的2款研制管線藥物ARC-520和ARC-521的研討發展,其原理是經過RNA攪擾作用來關閉乙肝病毒某些蛋白的表達,導致病毒無法增殖,然后再利用人體免疫系統對剩下病毒進行鏟除,完成免疫清潔狀況(immune clearant state),使得乙肝表面抗原(HBsAg)血清學轉陰或消失,具有功用性治好乙肝的潛力。
Arrowhead近來在2015年美國肝病研討協會年會(AASLD2015)發布了最新數據:ARC-520結合公司兩種特別siRNA序列(dynamic polyconjugate ,DPC),它們都經過特別潤飾,具有更好的穩定性與靶向性,在動物模型中可有用下降cccDNA(宿主細胞內的HBV cccDNA是病毒賴以仿制生計的要害)水平。不過,該藥物還未進行正式的人體臨床試驗。
(4)新式核苷類逆轉錄酶按捺劑TAF。
近來,吉祥德抗病毒管線再次傳來特大喜訊,該公司在研的另一種抗病毒藥物TAF在醫治乙肝(HBV)的2個III期臨床(Studies 108、110)獲得成功,達到了研討的首要結尾。吉祥德已計劃在2016年第一季度向美國和歐盟提交TAF醫治乙肝的上市請求。
TAF的優勢:低于Viread的1/10劑量時,就具有十分高的抗病毒作用。
Viread歸于新式核苷酸類逆轉錄酶按捺劑,是抗緩慢乙肝藥物的重要發展,經過攪擾乙肝病毒DNA聚合酶的功用按捺乙肝病毒的仿制,下降血清及肝安排內的病毒載量。
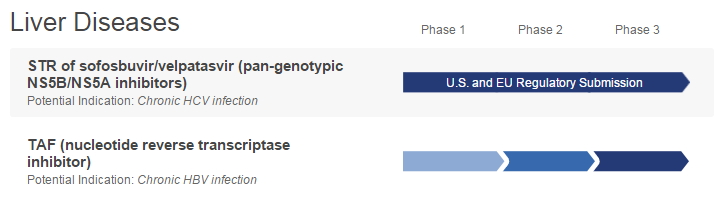
吉列德公司的TAF發展。
替諾福韋(tenofovir alafenamide fumarate,TAF)是一種新式核苷類逆轉錄酶按捺劑(NRTI),作為一種新組成的替諾福韋磷酸化前藥,每日口服一次,其血漿穩定性比Viread更好,進入乙肝感染的細胞后仍能堅持最大程度的完整性。且在之前的臨床試驗中,該藥已被證明在低于Viread的1/10劑量時,就具有十分高的抗病毒作用,一起可改進腎功用和骨骼方面參數。
TAF的遠景,或將替代Viread。
現在被使用于人類免疫缺點病毒(HIV)和乙型肝炎病毒(HBV)等的病毒感染性疾病。吉祥德公司保存Viread在香港、新加坡、韓國和臺灣地區的獨有上市權;葛蘭素史克保存Viread在我國上市的獨有上市權力,而且擔任Viread用于醫治HBV的注冊,Viread在2014年的銷售額達到了11億美元。分析師估量:TAF有望替代Viread,成為吉祥德穩固其在感染性肝炎醫治范疇領導者位置的利器。
關于TAF2個III期研討:Study 108和Study 110。
此次發布的2個III期研討均為隨機、雙盲、96周III期臨床研討,在1298例既往未承受醫治(初治)和已承受醫治(經治)的乙肝(HBV)成人患者中展開。
研討點評了TAF(25mg劑量)用于既往未承受醫治(初治)和現已承受醫治(經治)的乙肝e抗原(HBeAg)陰性乙肝患者、HBeAg陽性乙肝患者的效果和安全性。依據醫治48周時完成HBV DNA水平<29 IU/mL的患者份額,研討數據證明了TAF相對于吉祥德抗病毒藥物Viread的非劣效性;與Viread比較,TAF還改進了腎功用和骨骼安全參數。這2個研討的具體數據也將在未來舉行的科學會議上發布。
首要結尾:完成血漿HBV DNA水平<29 IU/mL的患者份額。
Study 108中,425例乙肝e抗原(HBeAg)陰性乙肝患者以2:1的份額,隨機承受TAF(n=285)或Viread(n=140)醫治。數據顯現,在研討的第48周,TAF醫治組完成HBV DNA水平<29 IU/mL的患者份額為94.0%(n=268/285),Viread醫治組數據為92.9%(n=130/140),達到了非劣效性首要結尾(CI -3.6% - +7.2%,p=0.47)。
Study110中,873例乙肝e抗原(HBeAg)陽性乙肝患者以2:1的份額,隨機承受TAF(n=581)或Viread(n=292)醫治。數據顯現,在研討的第48周,TAF醫治組完成HBV DNA水平<29 IU/mL的患者份額為63.9%(n=371/581),Viread醫治組數據為66.8%(n=195/292),達到了非劣效性首要結尾(CI -9.8% - +2.6%,p=0.25)。
要害非必須結尾:48周時髖關節和脊柱骨礦物質密度從基線的改變,48周時血清肌酐(ALT)從基線的改變。
2個研討中,在第48周時,與Viread醫治組比較,TAF醫治組髖關節和脊柱骨礦物質密度從基線取得了明顯更小的均勻百分比降幅(p<0.001)。闡明腎功用和骨骼參數改變方面,TAF計劃優于Viread計劃。
研討中,選用中心實驗室cut-off值和美國肝病研討協會(AASLD)2種規范來點評血清ALT水平的正常化。當選用AASLD規范點評時,與Viread醫治組比較,TAF醫治組在ALT正常化體現出統計學含義的明顯進步;當選用中心實驗室cut-off值(界說正常化在一個較高的ALT水平)點評時,2個醫治組ALT正常化無統計學明顯差異。
Study110研討中,TAF醫治組調查到了較小的血清肌酐增幅(p=0.02)。此外,2個研討中,估量的腎小球濾過率(eGFR)從基線到48周的中位改變,有利于TAF組(p<0.01)。
安全性點評:因不良反應停藥。
Study108研討中,TAF組為0.7%(n=2),Viread組為0.7%(n=1);Study 110研討中,TAF組為1.0%(n=6),Viread組為1.0%(n=3)。
2個研討中,最長陳述的不良反應包含頭痛、上呼吸道感染、咽炎、咳嗽,TAF組發生率與Viread組類似。
補白:本文部分翻譯參閱Medsci。
文章信源:
Gilead Announces Top-Line Results From Two Phase 3 Studies Evaluating Tenofovir Alafenamide (TAF) for Patients With Chronic Hepatitis B Infection。
Arrowhead Reports Fiscal 2015 Year End Results。
